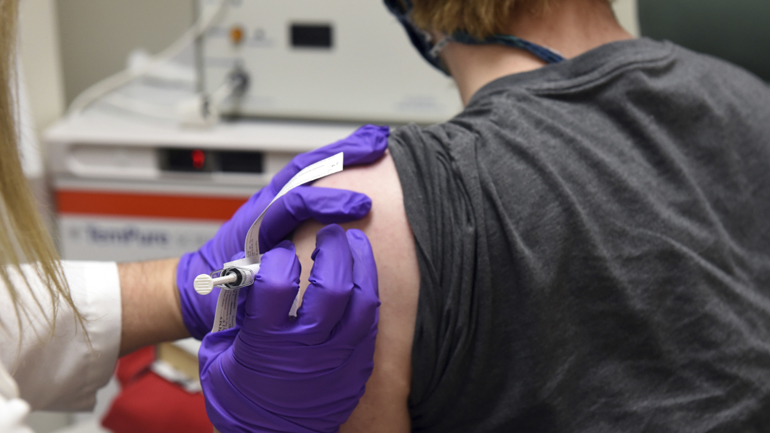
Τα στοιχεία τα οποία επικαλούνται οι εταιρείες Pfizer/BioNTech στην αίτηση τους προς τις αρχές των ΗΠΑ για την αδειοδότηση του εμβολίου τους, αποκαλύπτει σε ανάρτησή του ο καθηγητής κ. Ηλίας Μόσιαλος.
Συγκεκριμένα ο καθηγητής Πολιτικής της Υγείας του LSE αναφέρει τα ακόλουθα:
Νεότερα για την αίτηση επείγουσας αδειοδότησης του εμβολίου των Pfizer/BioNTech
Οι Pfizer/BioNTech θα υποβάλουν σήμερα την αίτηση έκτακτης αδειοδοτησης του υποψηφίου Covid-19 εμβολίου τους, στις ρυθμιστικές υγειονομικές αρχές των ΗΠΑ (FDA).
Η υποβολή του φακέλου βασίζεται:
1. στο ποσοστό αποτελεσματικότητας του εμβολίου- 95% (p <0,0001)- που καταδεικνύεται στην κλινική μελέτη φάσης 3 των εταιρειών σε συμμετέχοντες χωρίς προηγούμενη λοίμωξη SARS-CoV-2 (πρώτος πρωταρχικός στόχος) και επίσης σε συμμετέχοντες με και χωρίς προηγούμενη SARS -CoV-2 μόλυνση (δεύτερος πρωταρχικός στόχος), σε κάθε περίπτωση που μετράται 7 ημέρες μετά τη δεύτερη δόση.
2. Η ανάλυση βασίστηκε σε 170 επιβεβαιωμένες περιπτώσεις COVID-19.
3. Η υποβολή της αίτησης υποστηρίζεται επίσης από ζητούμενα δεδομένα ασφαλείας από ένα τυχαιοποιημένο υποσύνολο περίπου 8.000 συμμετεχόντων ηλικίας ≥18 ετών, και ανεπιθύμητα δεδομένα ασφαλείας από περίπου 38.000 συμμετέχοντες σε δοκιμές (που παρακολουθήθηκαν για διάμεσο διάστημα δύο μηνών μετά τη δεύτερη δόση του υποψηφίου εμβολίου).
4. Η υποβολή περιλαμβάνει επίσης ζητούμενα δεδομένα ασφαλείας για περίπου 100 παιδιά ηλικίας 12-15 ετών.
5. Περίπου το 42% των παγκόσμιων συμμετεχόντων και το 30% των συμμετεχόντων στις ΗΠΑ στη μελέτη Φάσης 3, έχουν διαφορετικά φυλετικά και εθνικά υπόβαθρα, ενώ στο 41% του παγκόσμιου και στο 45% των ΗΠΑ οι συμμετέχοντες είναι 56-85 ετών.
6. Μέχρι σήμερα, η Επιτροπή Παρακολούθησης των Δεδομένων (DMC) της μελέτης δεν έχει αναφέρει σοβαρές ανησυχίες για την ασφάλεια που να σχετίζονται με το εμβόλιο.
Σύμφωνα με πηγές του ειδησεογραφικού πρακτορείου Reuters, η επιτροπή του FDA σκοπεύει να συνεδριάσει τον Δεκέμβριο (8-10/12) για να συζητηθεί το εμβόλιο, αν και οι ημερομηνίες θα μπορούσαν να αλλάξουν.
Τι άλλο γνωρίζουμε;
1. Οι εταιρείες αναμένουν ότι το FDA θα χορηγήσει την άδεια έως τα μέσα Δεκεμβρίου.
2. Η Pfizer δήλωσε ότι αναμένει να ετοιμάσει 50 εκατομμύρια δόσεις εμβολίου φέτος, αρκετές για την προστασία 25 εκατομμυρίων ανθρώπων.
3. Ενα πιλοτικό πρόγραμμα δοκιμαστικής διανομής έχει ήδη ξεκινήσει σε 4 πολιτείες των ΗΠΑ.
Αυτή η εβδομάδα συνεχίζει με καλά νέα από το μέτωπο των εμβολίων και μένουμε αισιόδοξοι.
Νεότερα για την αίτηση επείγουσας αδειοδότησης του εμβολίου των Pfizer/BioNTech Οι Pfizer/BioNTech θα υποβάλουν…
Δημοσιεύτηκε από Ηλίας Μόσιαλος στις Παρασκευή, 20 Νοεμβρίου 2020